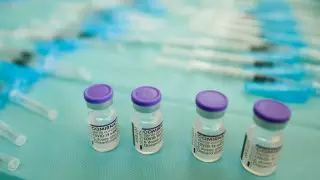
Главный санитарный врач Казахстана Ерлан Киясов утвердил методические рекомендации к вакцинации препаратом "Комирнати" (Pfizer, США), передает Tengrinews.kz.
В документе отмечается, что "Комирнати" - вакцина против коронавируса на основе мРНК (модифицированная нуклеозидами) для профилактики коронавирусной инфекции, вызываемой SARS-CoV-2. "Комирнати" не содержит вирус для выработки иммунной защиты, не может вызвать коронавирусную инфекцию.
Один флакон содержит 6 доз по 0,3 миллилитра после разведения.
В одной дозе (0,3 миллилитра) содержится 30 микрограммов вакцины против КВИ (BNT162b2) на основе мРНК (инкапсулированной в липидные наночастицы) и вспомогательные вещества.
Вакцинации подлежат:
- подростки в возрасте 12 лет и старше;
- беременные женщины - с 16-й по 37-ю недели беременности;
- женщины в период лактации - после окончания послеродового периода (через 42 дня).
Главный санврач страны подчеркнул, что перед проведением вакцинации обследование на наличие коронавируса и антител к коронавирусу не проводится.
Переболевшие подлежат вакцинации против КВИ через 6 месяцев после выздоровления с учетом оценки состояния перед вакцинацией. Допускается вакцинация переболевших через 3 месяца после выздоровления.
Противопоказания к введению вакцины:
- аллергия на действующее вещество или любые другие компоненты препарата; наличие аллергии на яйца или желатин не является противопоказанием или предостережением для вакцинации, так как вакцина не содержит эти компоненты.
- возраст до 12 лет;
- беременность до 16-й недели.
- лицам с известной в анамнезе тяжелой аллергической реакцией на полиэтиленгликоль или родственные молекулы, поскольку полиэтиленгликоль является компонентом вакцины.
Вакцинация проводится с осторожностью при:
- наличии тяжелой аллергической реакции или проблем с дыханием после введения какой-либо другой вакцины или после введения "Комирнати" в прошлом;
- падениях в обморок, судорогах после любой инъекции/укола;
- острых инфекционных заболеваниях с высокой температурой и обострениях хронических заболеваний;
- наличии проблем со свертыванием крови, в том числе прием лекарств против образования тромбов;
- ослабленная иммунная система из-за болезни (ВИЧ-инфекция, прием стероидных препаратов).
Срок хранения
Срок хранения невскрытых замороженных флаконов - 9 месяцев с момента производства только при температуре от минус 90 градусов до минус 60.
При переходе вакцины с температурного режима от минус 90 до минус 60 (уровень замораживания) на температурный режим от плюс 2 до плюс 8 (уровень размораживания) срок хранения вакцины составляет 31 день со дня и времени перехода.
В течение срока годности длительностью 9 месяцев невскрытые флаконы можно хранить и транспортировать при температуре от минус 25 до минус 15 в течение единого периода до двух недель, а затем помещать обратно в условия хранения при температуре от минус 90 до минус 60.
Вакцина хранится в оригинальной упаковке для защиты от света.
Рекомендации по применению вакцины "Комирнати"
Вакцинация проводится двукратно с интервалом 21-28 дней после первой дозы; рекомендуется использовать один и тот же препарат для введения обеих доз; в случаях, когда вторая доза случайно введена менее чем через 21 день, дополнительная доза не вводится.
В случае введения двух доз, если случайно были использованы разные вакцины, не рекомендуется введение дополнительной дозы любой из использованных вакцин.
Вакцина вводится после разведения в виде внутримышечной инъекции в дозе 0,3 миллилитра в дельтовидную мышцу (верхнюю треть наружной поверхности плеча); при невозможности введения в дельтовидную мышцу препарат вводят в латеральную широкую мышцу бедра.
Вакцина предназначена только для внутримышечного введения. Строго запрещено внутривенное введение препарата.
Размороженный флакон переносят в комнатную температуру, но не более чем на два часа, доводят до комнатной температуры и аккуратно переворачивают 10 раз перед разведением. Не встряхивать! До разведения размороженная дисперсия может содержать непрозрачные аморфные частицы белого или почти белого цвета.
Растворитель вакцины - раствор натрия хлорида для инъекций с концентрацией 9 мг/мл (0,9 процента) - хранится при комнатной температуре.
Размороженную вакцину разводят в оригинальном флаконе с помощью 1,8 миллилитра 0,9-процентного раствора натрия хлорида в асептических условиях; на один флакон вакцины используется одна ампула указанного растворителя (при разведении вакцины обеспечивается одинаковая температура вакцины и растворителя).
Перед извлечением иглы из пробки флакона выравнивают давление во флаконе путем вытягивания 1,8 миллилитра воздуха в пустой шприц для разведения.
Разведенную вакцину (дисперсию) 10 раз аккуратно переворачивают. Не встряхивать! Разведенная вакцина должна представлять собой дисперсию почти белого цвета. При наличии частиц или в случае изменения цвета разведенную вакцину не используют.
После разведения на флаконе следует указать соответствующие дату и время.
После разведения вакцину следует хранить при температуре от плюс 2 до плюс 30 и использовать в течение 6 часов.
Не замораживать и не встряхивать разведенную вакцину.
Для разведения вакцины используется шприц от 2 до 5 миллилитров, градуированный с шагом 0,1 миллилитра.
Для введения вакцины используется саморазрушающийся (самоблокирующийся) шприц объемом 0,3 или 1,0 мл, градуированный с шагом 0,1 мл.
После разведения флакон содержит 2,25 миллилитра вакцины, и из него можно извлечь 6 доз по 0,3 мл. В асептических условиях очищают пробку флакона одноразовым антисептическим тампоном, извлекают 0,3 мл препарата с помощью шприца; для извлечения 6 доз из одного флакона следует использовать шприцы и (или) иглы с малым "мертвым" объемом. Совокупный малый "мертвый" объем шприца и иглы должен составлять не более 35 мкл. Перед каждым набором доз переворачивание флакона не требуется.
Перед введением вакцины необходимо продезинфицировать кожу 70-процентным раствором спирта; перед введением вакцины необходимо убедиться в том, что спирт полностью испарился с поверхности кожи.
Объем каждой дозы вакцины для введения прививаемому должен составлять 0,3 миллилитра.
К использованию непригодна вакцина с нарушенной целостностью и/или маркировкой флакона, при изменении физических свойств (мутность, окрашивание), неправильном хранении и/или с истекшим сроком годности.
Рекомендуется соблюдать интервал между вакцинацией против КВИ с применением вакцины "Комирнати" и вакцинацией другими прививками не менее 14 дней.
Вакцина "Комирнати" у некоторых прививаемых может вызывать следующие ожидаемые реакции:
- очень часто (могут возникать у более чем 1 человека из 10): боль, припухлость в месте инъекции, утомляемость, головная боль, мышечная боль, боль в суставах, озноб, диарея, лихорадка; некоторые из перечисленных реакций у подростков в возрасте от 12 до 15 лет встречались несколько чаще, чем у взрослых;
- часто (могут возникать не более чем у 1 человека из 10): покраснение в месте инъекции, тошнота, рвота;
- нечасто (могут возникать не более чем у 1 человека из 100): увеличенные лимфоузлы, недомогание, боль в руке, бессонница, зуд в месте инъекции, аллергические реакции, такие как сыпь или зуд;
- редко (могут возникать не более чем у 1 человека из 1000): временный односторонний паралич лицевого нерва, аллергические реакции, такие как крапивница или отек лица;
- неизвестно (исходя из имеющихся данных частоту возникновения определить невозможно): тяжелая аллергическая реакция, воспаление сердечной мышцы (миокардит) или воспаление наружной оболочки сердца (перикардит), которое может привести к одышке, учащенному сердцебиению или боли в груди, обширная отечность в месте инъекции с распространением на всю конечность, отечность лица, если в прошлом были сделаны косметические инъекции в область лица.
Отметим, нами выборочно приводятся лишь некоторые выдержки из официальных рекомендаций главного санврача. Полную версию документа можно найти на сайте Комитета санитарно-эпидемиологического контроля Минздрава.